23 сентября 2021 г
Новый препринт описывает значительные различия в раннем иммунном ответе, вызванном двумя из самых ранних вакцин, для получения экстренного разрешения против коронавирусной болезни 2019 (COVID-19).
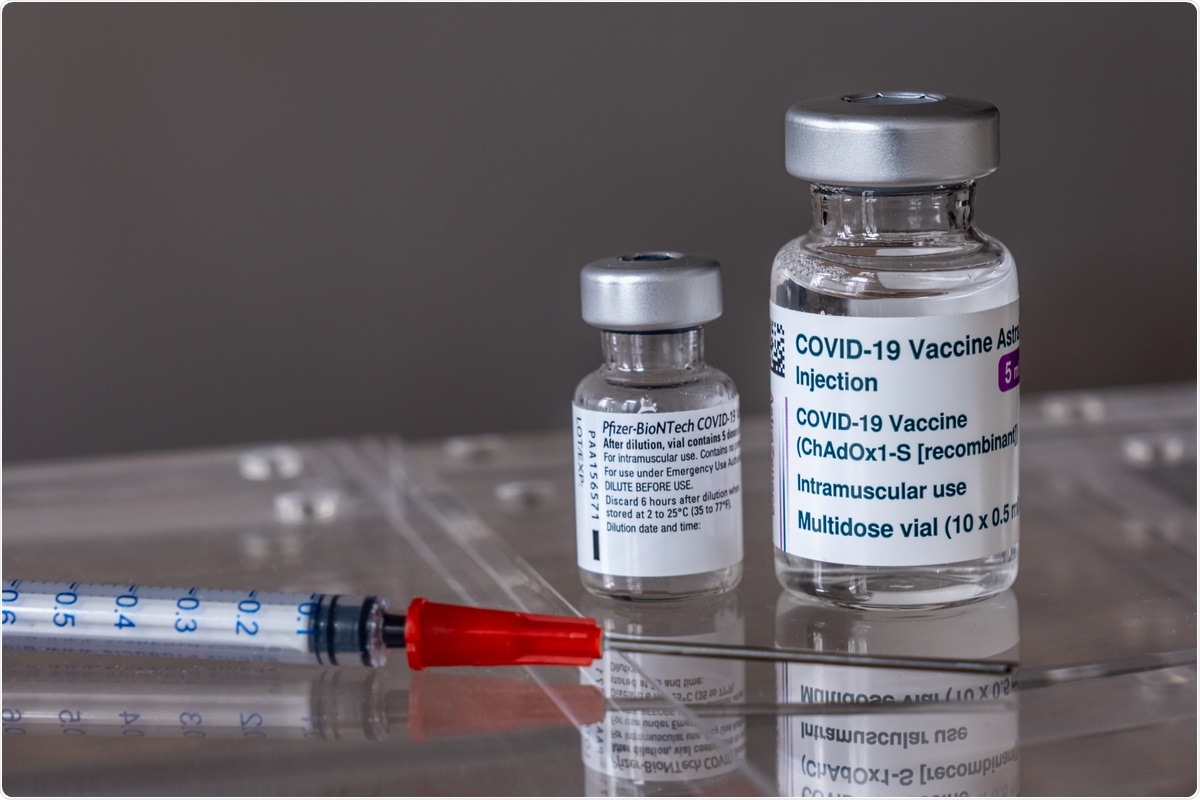 Исследование: однодозовая вакцинация SARS-CoV-2 с BNT162b2 и AZD1222 индуцирует расщепление ответов Th1 и производство IgA. Изображение предоставлено: Марк Брюксель / Shutterstock
Исследование: однодозовая вакцинация SARS-CoV-2 с BNT162b2 и AZD1222 индуцирует расщепление ответов Th1 и производство IgA. Изображение предоставлено: Марк Брюксель / Shutterstock
Предварительная версия исследования доступна на сервере medRxiv *, в то время как статья подвергается рецензированию.
Фон
Вакцинация COVID-19 направлена на выявление выработки антител, нацеленных на шиповой антиген SARS-CoV-2, нейтрализуя его связывание с рецептором ангиотензинпревращающего фермента 2 (ACE2) на клетке-хозяине, чтобы ингибировать его попадание в клетку-хозяин для установления инфекции ,.
Текущее исследование касается двух таких вакцин:
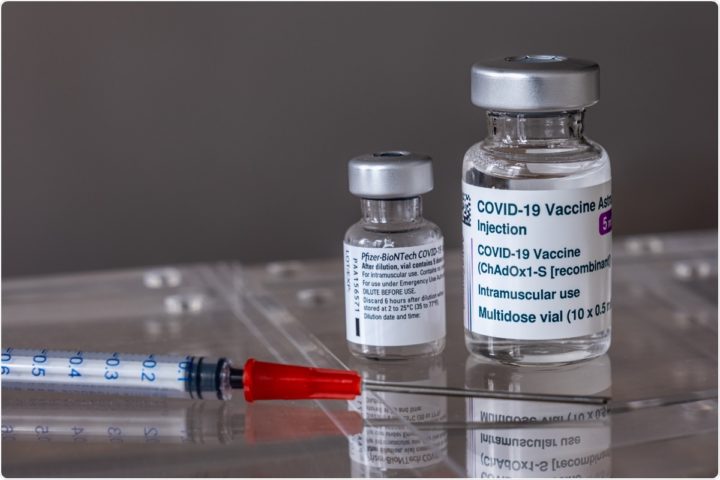
- аденовирусный вектор первого поколения AZD1222 (от AstraZeneca), который использует аденовирус сим-ДНК ChAdOx1 для доставки всплеска вируса реципиенту вакцины
- вакцина Pfizer / BioNTech BNT162b2 на основе мессенджер-рибонуклеиновой кислоты (мРНК), окутанная липидными наночастицами. МРНК кодирует шиповой антиген для трансляции в клетках-реципиентах.
Обе эти вакцины связаны с эффективной защитой от симптоматической и тяжелой COVID-19 после двух доз. Самые ранние данные указывают на высокую эффективность после одной дозы. Появились варианты вируса с множественными мутациями шипа, которые вызывают большую потерю эффективности вакцины (VE).
Исследователи хотели изучить молекулярные и клеточные иммунные ответы, возникающие после одной дозы любой вакцины. Поэтому они изучали частоты различных лейкоцитов в периферической крови, участвующих в врожденном и адаптивном иммунитете, отслеживая изменения в их количестве в течение первых трех недель после вакцинации. Они также рассмотрели нацеленные на шипы антитела к иммуноглобулину в плазме, в дополнение к выработке и активности специфических для шипа Т-клеток-эффекторов.
Что показало исследование?
Исследователи обнаружили, что обе вакцины производят разные типы и титры опосредованных антителами и клетками иммунных реакций после одной дозы.
Вначале лейкоциты в крови снижались более чем в два раза после одной дозы вакцины AZD1222, главным образом из-за снижения количества гранулоцитов, В-клеток и CD4- и CD8-83-положительных Т-клеток. Эти подсчеты были полностью восстановлены к 13 дню. Провоспалительные моноциты также были выше на 2-й день в этой группе. С гранулоцитами маркеры CD14 + CD16 + были повышены в это время.
Такие изменения не были зарегистрированы после вакцины BNT162b2, что указывает на то, что, в отличие от вакцины AZD1222, она не вызывала значительных изменений в количестве или частотах врожденных иммунных клеток, гранулоцитов или моноцитов.
На 13-й день после вакцинации BNT162b2 было обнаружено, что плазмабласты достигают пика со средним значением 1,6% по сравнению с шестым пиком дня со средним значением 3% после вакцины AZD1222. Было обнаружено, что экспрессия CD27 и CD38 на CD8 + T-клетках смещается в сторону терминальной дифференцировки цитотоксических T-клеток в это время.
Также на 20-й день было обнаружено, что Т-клетки CD4 + CD127 – CD27 + эфекторной памяти имеют более высокую частоту, что снова указывает на сдвиги как В, так и Т-клеток после AZD1222, но не BNT162b2.
Когда белые клетки из конвалесцентов COVID-19 или полностью вакцинированных индивидуумов стимулировались либо рекомбинантным белком шипа, либо вакциной на основе шипа BNT162b2, было обнаружено, что первая вызывает активацию CD4 + T-клеток. Последнее привело к активации лимфоцитов CD4 + и CD8 +.
Связанные истории
- Исследователи сообщают о недостаточно последовательной области гена S варианта дельты SARS-CoV2
- Естественная инфекция SARS-CoV-2 вызывает более длительный иммунитет, чем предполагает исследование вакцинации
- Фаза I исследования исследует использование антипаразитарного нитазоксанида для лечения COVID-19
Гамма-интерферон (IFNγ) -продуцирующие клетки были значительно увеличены после вакцинации BNT162b2, но не с AZD1222.
Более поздние ответы
Адаптивные ответы после любой вакцины показали, что иммунный ответ также прогрессирует до фенотипа Т-клеток эффектора с увеличенными CD8 + CD137 + Т-клетками, которые также экспрессировали маркер CD25 (IL-2Rα). Специфичные для шипов цитотоксические эффекторы Т-клетки также были расширены, причем более высокие пропорции клеток FasL + CD8 + появлялись после рестимуляции мРНК шипа
Вакцина AZD1222 привела к увеличению IFNγ-продуцирующих CD8 + T-клеток, но сократила регуляторные CD8 + клетки и противовоспалительное совместное производство IL-2 и IL-10 в клетках CD4 + и CD8 +.
Эффекторные Т-хелперные клетки также были увеличены с обеими вакцинами, но только AZD122 был связан с повышенными провоспалительными TNFα-продуцирующими хелперными CD4 + Т-клетками. Т-клетки-помощники типа 2, специфичные для антигена шипа, заметно отсутствовали после любой вакцины.
Таким образом, одна доза любой вакцины привела к расщеплению CD4 + и CD8 + эффекторных Т-клеток, хотя изменения были более очевидными после AZD1222.
Ответы антител
В то время как AZD1222 преимущественно индуцировал IgM и IgG, без обнаруживаемой продукции IgA, до 20-го дня после вакцинации BNT162b2 вызывал небольшое количество IgM, но с более высоким увеличением титров IgG и IgA.
Каковы последствия?
Ранняя иммунная реакция после первичной дозы AZD1222 или BNT162b2 включает сильные клеточные и опосредованные антителами ответы, но с различными паттернами. В то время как первый вызвал падение периферических лейкоцитов на 2-й день, включая гранулоциты и В или Т-клетки, это связано с аденовирусным вектором. Другие изменения, связанные с AZD1222, также соответствуют этой картине, такие как временное увеличение воспалительных моноцитов.
Известно, что коммутируемый ответ класса поздней фазы с клетками памяти В, наблюдаемыми после одной дозы этой вакцины, связан с высокой противовирусной защитой. Таким образом, аденовирусный вектор, вероятно, вызывает эти периферические иммунные реакции, а не спайковый антиген SARS-CoV-2.
Вакцинация BNT162b2 вызвала менее поразительный ответ, что указывает на то, что она лучше переносится. МРНК вакцины была разработана для ослабления ее обнаружения врожденными иммунными клетками. Небольшое увеличение частоты плазмабластов после этой вакцины может быть связано с адаптивным иммунитетом к белку шипа, в отличие от более крупного роста, наблюдаемого с AZD1222, вызванного сочетанием аденовирусных и речевых реакций.
Сильный ответ IgA с вакцинацией BNT162b2 может указывать на причину его лучшей симптоматической защиты COVID-19. Конструкция вакцины должна обеспечивать иммунитет слизистой оболочки, чтобы обеспечить IgA и активацию клеток-эффекторов, резидентных тканей, для предотвращения инфекции слизистой оболочки носоглотки.
В то время как обе вакцины расширили эффекторные Т-клетки аналогичным образом, AZD1222 индуцировал ответ Th1-скеведа, который может помочь обеспечить сильный клеточный иммунитет к антигену шипа. И наоборот, подавляющий ответ Th1 может привести к секретному профилю цитокинов, который ингибирует переключение классов в направлении производства IgA.
Тем не менее, BNT162b2 также индуцировал IFNγ-продуцирующие T-хелперные клетки, специфичные для шипа, сильнее, чем AZD1222. Необходимы дальнейшие исследования, чтобы установить, способствует ли BNT162b2 производству IgA.
Ответ Th1 является общим для обеих вакцин. Значительное снижение IL-10 может, возможно, привести к постоянному отклику Th1, создавая среду, которая ингибирует выработку IgA.
*Важное уведомление
medRxiv публикует предварительные научные отчеты, которые не являются рецензируемыми и, следовательно, не должны рассматриваться как убедительные, руководящие клинической практикой / поведением, связанным со здоровьем, или рассматриваться как установленная информация.
Ссылка на журнал:
Мюллер М. и соавт. (2021) «Вакцинация SARS-CoV-2 с одной дозой с BNT162b2 и AZD1222 с индуцированным расщеплением ответов Th1 и производства IgA». medRxiv. DOI: 10.1101 / 2021.09.17.21263726.